北京基因組研究所(國家生物信息中心)合作揭示年輕血液促進干細胞及機體年輕化的分子機制
衰老是一種涉及全身多種組織器官系統性退化的過程,表現為漸進性機體再生能力減弱及功能衰退。異體共生(Heterochronic parabiosis)是通過外科手術連接年老和年輕小鼠的循環系統所構建的模型。可用于評價老化的機體受年輕血液影響后如何恢復活力,反之亦可用于研究年輕的組織和器官受衰老血液影響后加速退行。年輕血液究竟靠何種力量使衰老個體重返“年輕態”的秘密還有待揭示。相關的重要科學問題包括:哪些衰老的器官、組織和細胞類型可以或者更容易被年輕血液“返老還童”?衰老干細胞的活力是否能被年輕血液增強?能否發現介導年輕血液效應的“年輕因子”,并以此作為干預器官衰老的新型分子靶標?
2022年5月24日,中國科學院北京基因組研究所(國家生物信息中心)張維綺研究組同中國科學院動物研究所劉光慧研究組、曲靜研究組合作,于Cell Stem Cell雜志在線發表題為“Heterochronic parabiosis induces stem cell revitalization and systemic rejuvenation across aged tissues”的研究論文。該研究通過構建年老小鼠和年輕小鼠的異體共生模型,繪制了系統水平的單細胞轉錄組圖譜,并對骨髓、脾臟、外周血、腦、肝臟、骨骼肌和皮膚等7種組織器官進行了深入解析。
研究發現,暴露于年老個體的血液可以使年輕個體的不同器官、組織和細胞類型呈現加速衰老的特征。而年老個體受年輕血液影響則呈現出典型的“年輕化”改變,主要表現為衰老組織微環境的改善及相應干(祖)細胞的激活。被激活的干(祖)細胞群體包括皮膚的基底細胞和毛囊干細胞、骨骼肌的成纖維/脂肪祖細胞,以及定位于骨髓的HSPC。其中,衰老的HSPC對年輕血液的反應尤為敏感。結合差異基因表達、核心調控轉錄因子和細胞-細胞間通訊分析,研究團隊發現了一系列以表觀調控基因YY1以及細胞趨化因子CCL3為代表的HSPC衰老調控因子。結果顯示,YY1的表達降低與HSPC老化密切相關,但其表達水平對年輕血液刺激缺乏足夠響應性,而在衰老HSPC中被抑制的CCL3則可以被年輕血液誘導激活。進一步的小鼠移植實驗發現,慢病毒介導的YY1過表達可有效增強年老的造血干(祖)細胞的重建能力;而基于CCL3過表達的“基因療法”可顯著提高年老造血干(祖)細胞向淋系分化的能力。上述研究表明,暴露于年輕血液可有效改善老年個體不同器官的組織微環境,并恢復多種成體干細胞的活力。其中,造血干(祖)細胞(HSPC)是對年輕血液尤為敏感的細胞類型之一,年輕的血液可以通過上調趨化因子CCL3的表達促進衰老HSPC的“年輕化”。
該研究以單細胞分辨率、跨器官、多維度的形式系統解析了異體共生模型中年輕血液促使老年個體“年輕化”以及年老血液加速年輕個體“老化”的細胞分子變化規律,揭示了年輕體內環境促進年老組織再生的關鍵介導因子,為發展衰老預警和干預的關鍵標志物和新型策略提供了豐富的數據資源以及重要線索和思路。同時,該工作也為從系統生物學角度發現機體“年輕化因子”提供了新的研究范式,在科學應對老齡化方面具有潛在的應用價值。
該項研究由中科院動物所、中科院北京基因組所、中科院干細胞與再生醫學創新研究院、北京干細胞與再生醫學研究院、首都醫科大學宣武醫院、清華大學、中國農業大學、北京協和醫院等機構合作完成。中科院動物所劉光慧研究員、中科院北京基因組研究所張維綺研究員、和中科院動物所曲靜研究員為共同通訊作者。中科院動物所馬帥副研究員、首都醫科大學宣武醫院王思研究員、中科院動物所葉燕霞助理研究員、中科院北京基因組研究所任捷研究員以及清華大學陳瑞輕博士為并列第一作者。研究得到清華大學王建偉教授、首都醫科大學宣武醫院陳彪教授、中科院動物所宋默識研究員、中國農業大學于舒洋教授的合作及支持。該研究獲得科技部、國家自然科學基金委、中國科學院和北京市科委等項目資助。
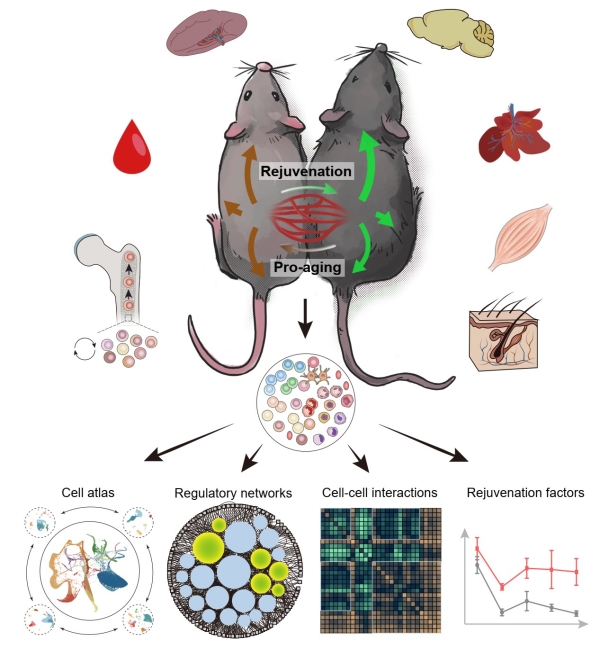
年輕血液促進機體多組織年輕化的系統生物學研究
附件下載: